
真实的证据,或者莱茵集团,是根本上改变未来的医疗保健。这是如何发生的:
- 真实数据(RWD)聚合和变成了RWE健壮的分析。
- 真实的证据(RWE)提供clinically-rich见解在日常实践和为什么实际上发生了什么。
- 利益相关者在整个医疗系统使用这个新的知识来支持决策,提高安全性和有效性,最终,病人的结果。
让我们仔细看看RWD,它变成了RWE和RWE整个医疗生态系统的价值通过九个用例。
在这篇文章中我们将介绍:
- 现实世界的数据(RWD)是什么?
- 真实的证据(RWE)是什么?
- 为什么我们需要真实的证据?
- 使用真实的证据在制药和设备公司
- 监管机构中使用真实的证据
- 使用真实的证据在临床医生和学术研究人员
- 在卫生保健系统使用真实的证据
- 注册中心的作用产生真实的证据
现实世界的数据(RWD)是什么?
为了了解真实的证据及其在医疗保健作用,我们必须首先定义真实世界的数据,或RWD。
真实的数据是任何数据收集的常规护理,而不是收集的数据在一个临床试验,研究设计控制变化的方式不能代表现实世界的保健和结果。
有许多不同的类型和RWD来源。让我们仔细看看每种类型,其来源,其用途。
- 临床数据 从电子健康记录(EHRs)和病例报告形式(eCRFs)。这些数据提供病人人口、家庭历史,并发症,手术和治疗的历史,和结果。
- 我们相信数据 从 patient-reported (PRO)的调查结果。这些数据直接从病人提供见解,他们帮助研究人员了解发生了什么以外的医院看病,过程和住院。
- 成本和使用数据 索赔和公共数据集。他们提供的信息关于医疗服务利用率,人口覆盖率,处方模式。
- 公共卫生数据 各种政府数据来源。这些关键信息添加到使利益相关者为了最好地服务于他们所服务的人群的需求。

真实的证据(RWE)是什么?
美国食品和药物管理局(FDA)将RWE定义为“临床证据关于使用和医疗产品的潜在益处和风险来源于真实世界数据的分析。”[1]
与传统的临床试验,可以策划和收集必要的数据元素授权,RWE的创建需要评估,验证和聚合不同,往往不同,数据来源可以通过常规临床实践。
RWE的创建需要的组合18.luck新利 、验证方法和一个健壮的知识可用的RWD来源(如现有质量注册中心中捕获的数据,哪些数据可以通过一个捕获EHR或索赔,病人组织捕获数据有关病人组)。
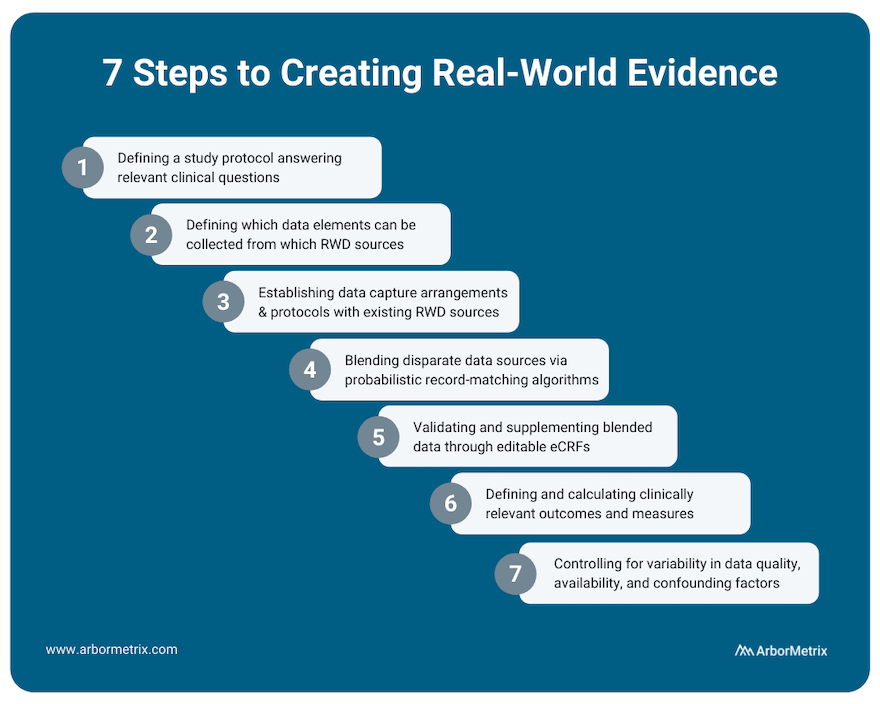
这个过程包括几个步骤:
- 定义一个研究方案回答相关临床问题。
- 定义数据元素可以被收集的RWD来源。
- 建立数据采集协议和协议与现有RWD来源。
- 通过概率记录匹配算法混合不同的数据源。
- 通过编辑eCRFs验证和补充混合数据。
- 定义和计算相关的临床结果和措施。
- 适当的评估和控制数据质量的变化,可用性和病人混杂因素影响测量结果。
RWE可以提供病人的整体观念,在很多情况下不能通过传统的临床试验研究。
为什么我们需要真实的证据?
有差距研究(我们学习)和日常实践(我们)在医疗保健、和它创建一个预计将发生什么和什么之间的区别真的发生了。
但它是什么真的重要的发生。驾驶可衡量的改进医疗保健需要扎根于我们所有人的现实实际发生之前,期间和之后的临床过程、干预、以及办公室访问。
RWE来填补这些差距和根我们的真理。它告诉我们真正当医生治疗范围广泛的病人,看起来不像同类病人组在临床试验中。
正因为如此,RWE许多用途,并提供很多好处在医疗保健服务的生态系统。
使用现实世界的证据在制药和设备公司
制药和医疗设备公司RWE的主要消费者,因为它可以提供价值在整个产品生命周期。
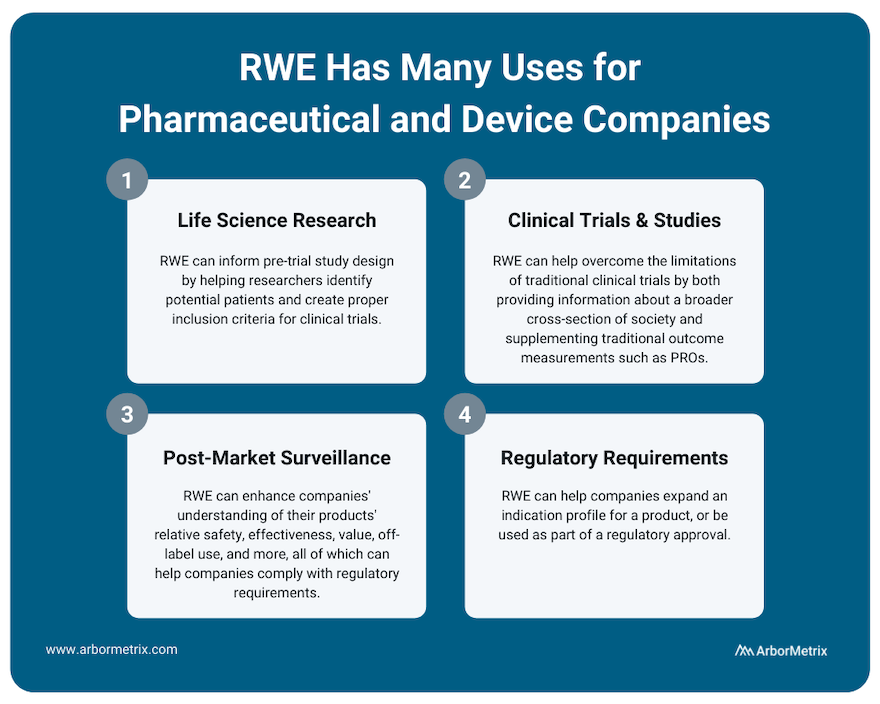
用例# 1:RWE和生命科学的研究(审前设计)
RWE研究起着重要的作用在整个产品生命周期对药品和设备公司。它可以告知审前研究设计,帮助研究人员识别潜在的患者,为临床试验创造适当的入选标准。
用例# 2:RWE和临床研究和试验
大部分医疗创新是由传统的临床试验,在新药品和设备严格研究和跟踪之前他们可以出售和广泛分布。尽管临床试验是非常重要的决定新技术的安全性和有效性,真实的证据相比,他们有一些限制。
例如:
- 传统临床试验可以有严格的入选标准,让供应商准确推断我们的临床试验结果更广泛的人口。
- 参与临床试验往往受限于研究管理员是谁能够招募,以及各种人口往往无法参与。这再一次挑战在患者群体的临床试验结果的普遍性。
真实的证据可以帮助克服临床试验的局限性,提供更广泛的社会领域的信息。这可以帮助临床医生、研究人员和行业合作伙伴更好的了解他们的产品和它们是如何工作的。
同时,在临床试验期间,RWE可以补充传统的测量结果与我们的数据等patient-reported结果(优点)或生物识别数据之间更容易收集医生预约。
用例# 3:RWE和上市后监测
一旦批准和销售产品,RWE可以帮助制药或医疗设备公司了解他们产品的相对安全,效率,价值,标示外使用等等。这上市后监测、上市后监测在医疗保健价值利益相关者。例如,我们支持一些临床数据登记提供实时RWE设备制造商用来评估他们的产品。
这个上市后监测的目的包括:
- 检测不良事件或在风险出现时实际使用的设备或药物。
- 比较新产品或与现有的选项和保健的标准治疗方法。
- 更新临床指南作为特定群体或团体找到比其他人更受益。
- 符合监管要求。
用例# 4:RWE和监管要求
RWE公司可以帮助企业扩大产品的说明资料。例如,虽然它可能不是可行的执行一个完整的临床试验的产品,常用药品核准标示外迹象,从疾病或产品注册,通过收集RWD公司可能能够为他们的研究成果和安全数据产品或设备,可以用来补充提交美国FDA和欧洲药品局(EMA)。
此外,美国食品和药物管理局已经表明,对某些产品,承诺上市后时期RWE分析可以使用的监管部门的批准。例如,它可能不是可行的临床试验运行在一个产品也被移植在很长一段时间。在这种情况下,上市后RWE可以帮助提供失踪的长期数据。
监管者之间使用现实世界的证据
美国食品及药物管理局等监管机构和EMA越来越多地使用真实的证据,并在某些情况下需要它,以满足上市后批准。
用例# 5:RWE和上市后的批准
美国食品及药物管理局提供了一个框架,提供了洞察力和指导如何利用RWE支持一个新的药物或设备监管申报文件中。[2]
他们特别注意几个用例RWD和RWE可以利用:
- 扩展标签显示的产品或设备。
- 上市后监测研究。
- Post-approval设备监测作为批准的条件。
- 对照组临床研究。
- 补充数据来帮助理解临床试验数据。
- 客观的性能标准和性能目标。
使用现实世界的证据在临床医生和学术研究者
用例# 6:RWE和决策支持工具
通过先进的分析,RWE可以提供个性化的决策支持工具,可以方便病人和医生之间的共享决策。例如,密歇根减肥手术协作使用一个工具,预测,基于个人特征,病人可能如何应对不同类型的减肥手术。
用例# 7:RWE和指导发展
通过比较结果为不同的治疗方案,它可能变得明显,特定的药物或剂量为不同的个体,更好的优化和治疗指南可以相应的细化和优化。
用例# 8:RWE和临床研究
有大量真实数据集,研究人员可以执行观测,回顾性和前瞻性研究,帮助其学术进步的理解当前的治疗方法和技术。看看这个列表研究出版物,RWE临床注册使用推进知识。
在卫生保健系统使用真实的证据
用例# 9:质量测量,基准测试和改进
RWE可以跟踪结果和质量措施跨组织。对于管理员,RWE可以提供整个卫生系统是如何执行的信息相对于其他人,以及个人的医生如何基准相对于同行。这些信息可以帮助通知覆盖与纳税人的讨论,和完善质量优先的补偿策略奖励坚实的成果。
注册中心的作用产生真实的证据
临床注册,包括病人、产品和要求注册,不仅提供丰富的RWD来源。他们也关键工具生成RWE本身和使用莱茵集团的支持上市后监测和研究。
如果你想阅读更多关于注册的角色在莱茵集团,看看这篇文章:这里有一个例子全球医疗器械注册表提供了真实的证据
